Водород из алюминия и воды. Получение водорода с использованием нанопорошка алюминия Реакция алюминия с выделением водорода

Всем привет, на этот раз мы проведем интересный эксперимент по превращению алюминия в топливо, коим выступает водород. Если вы смотрели вторую часть фильма «Назад, в будущее», то там был один интересный момент, когда доктор Эммет Браун «заправлял» Делореан.

В будущем техника уже давно работает на бытовых отходах, преобразуя всякий хлам в электроэнергию. Таким преобразователем в фильме является установка под названием «Мистер Фьюжн». Док выливает в аппарат остатки напитка, а также закидывает потом туда и алюминиевую банку. Вероятнее всего в качестве напитка там была Кока-кола.
Но как же с научной точки зрения можно получить энергию из таких отходов? Один автор решил повторить этот эксперимент, и у него получилось вполне неплохо. Что же скрывается за всем этим? Все на самом деле очень просто, энергию мы будем получать из алюминия, добывая из него водород. Делать это можно различными способами, алюминий является довольно таки не стойким металлом, если разрушить его оксидную пленку. Он начинает при этом выделять водород, просто контактируя с воздухом. Для разрушения оксидной пленки можно использовать кислоты и другие вещества. К примеру, можно просто поцарапать алюминий иголочкой под капелькой ртути и в этом месте оксидная пленка будет разрушена.
Зачем же при эксперименте будет нужна кока-кола, узнаете из статьи;)
Материалы и инструменты, которые использовал
Список материалов:
- шланги;
- доски;
- пластиковые бутылки;
- двухтактный двигатель;
- двигатель постоянного тока 12В;
- аккумулятор 12В;
- (по желанию);
- пластиковая канистра;
- манометр;
- металлические хомуты;
- кусок металлической трубочки;
- холодная сварка;
- активированный уголь;
- вода;
- тонкая листовая сталь;
- саморезы.
Для химической реакции: алюминий, кока-кола, гидроксид натрия.
Список инструментов:
- ножницы;
- шуруповерт;
- ножовка;
- ;
- ключи, отвертки и прочие мелочи.
Приступаем к сборке устройства:
Шаг первый. Теория
Суть в следующем, берем кока-колу и добавляем в нее гидроксид натрия. В кока-коле есть фосфорная кислота, при взаимодействии ее с гидроксидом натрия, получается вещество ортофосфат натрия, а также вода. Так вот, если в ортофосфат натрия добавить алюминий, получается бурная реакция с выделением водорода, который нам и нужен.
Все, что нам останется, это приспособить емкость для проведения реакции, а также установить фильтры и потребитель водорода, коим является ДВС.





Шаг второй. Устанавливаем «реактор»
В качестве основы вам понадобится кусок доски, прикручиваем к ней брусья для удерживания канистры. Канистра у нас работает в качестве реактора. Вокруг канистры намотайте резиновый шланг, он будет работать в качестве конденсатора, чтобы в двигатель не шел водяной пар.
В верхней части канистры устанавливаем манометр, а также штуцер для подключения шланга отвода газа.



Шланг от канистры подключаем к теплообменнику, а к выходу теплообменника подключается тоже кусок шланга с тройником. Один выход тройника задействуется для подключения горелки, в качестве которой выступает кусок металлической трубочки. Перед горелкой должен обязательно стоять кран, так как вы потом не сможете подать газ в двигатель.





Шаг третий. Установка фильтров
Фильтрующая система состоит из двух фильтров. Первый представляет собой бутылку с налитой внутрь водой, в которую опускается шланг от теплообменника. Этот фильтр предназначен для того, чтобы собирать крупные капли влаги, образующиеся в теплообменнике. Также с помощью этого фильтра можно наглядно наблюдать, как активно поступает газ в двигатель. Чтобы закрепить бутылку, отрежьте донышко от еще одной бутылки и закрепите его саморезами на основе. Теперь вставляем фильтр в этот кронштейн.



Что касается второго фильтра, тот тут уже происходит более тонкая очистка. В качестве фильтрующего элемента засыпьте внутрь бутылки активированный уголь. Шланги заводим через отверстия, которые сверлятся в крышках бутылок. Для герметизации можно использовать горячий клей или холодную сварку, как автор.









Шаг четвертый. Устанавливаем двигатель
Питать водородом мы будем двухтактный двигатель внутреннего сгорания. Подойдет мотор от бензокосы, бензопилы или другой подобной техники. Двигатель крепим винтами к бруску, который устанавливается на основу.
Двигатель нужно подготовить к работе на газу. Для этого нам понадобится небольшая пластиковая бутылочка. Вырезаем в крышке отверстия под винты и делаем входящее отверстие под карбюраторное. Крышку крепим к карбюратору. От бутылочки отрежьте донышко, а вместо него наденьте губку или что-то подобное, что подойдет на роль фильтра.
Проделайте у входа в карбюратор отверстие в бутылочке и установите шланг для подвода газа.












Очень важным моментом для работы двухтактного двигателя является система смазки. Тут автор нашел очень интересное решение, подача масла осуществляется в карбюратор, то есть, вместо бензина. При желании вы всегда можете отрегулировать нужное количество масла, которое будет поступать при работе ДВС. Определять, много масла льется или мало, можно по количеству дыма, также первое время нужно следить за тем, чтобы двигатель не перегрелся. Установите стойку, закрепите на ней емкость с маслом и подключите шланг к карбюратору.




В завершении устанавливаем двигатель на 12В, подключаем его к валу ДВС. В итоге у нас получается два в одном, это стартер, которым мы будем заводить движок, а также этот стартер будет работать как генератор электричества! Автор изначально планировал подключить через инвертор к генератору лампу на 110 Вольт, но инвертор оказался неисправным.
Валы генератор и двигателя соединяются с помощью куска резинового шланга. Для надежности вы можете вставить более тонкий шланг в более толстый. Фиксируем все это дело с помощью металлических хомутов.
После этого можно попробовать завести двигатель. Брызните на воздушный фильтр жидкости для запуска двигателя и подайте напряжение на двигатель, чтобы раскрутить ДВС. Не забывайте о зажигании и направлении вращения.












Шаг пятый. Приступаем к тестированию установки!
Сначала нужно заправить «Мистер Фьюжн», заливаем канистру кока-колу, у автора ушло 7 банок. Затем добавьте в колу гидроксид натрия и все перемешайте. Осталось добавить алюминий. Режем алюминиевые банки от колы на мелкие куски и засыпаем в канистру. Тут же начнется мощная реакция с выделением большого количества тепла и водорода. Закрываем крышу и ждем, пока не образуется нужное давление. Оно должно составлять минимум 2PSI (0.13 Атмосфер), чтобы газ можно было использовать. Но избегайте высокого давления, так как газ может запросто детонировать!
В процессе реакции выделяется столько тепла, что вода начинает кипеть. Чтобы этого избежать, автор поливает канистру холодной водой.
Метод довольно прост и способен дать Вам водород довольно быстро.
берем слиток алюминия, наносим на него шарик ртути, той что используется в обыкновенных градусниках. Берем острый предмет, например нож и царапаем им алюминий прямо под шариком ртути, то есть вводим в ртуть кончик ножа и царапаем под ним алюминиевый слиток, после этой операции у нас под шариком ртути получиться амальгама, то есть сплав ртути с алюминием, когда мы царапаем алюминий, то мы срываем с него защитный слой оксида алюминия.
В обычных условиях, на открытом воздухе алюминий сразу покрывается тончайшей, но очень прочной оксидной пленкой, эта пленка и препятствует дальнейшему окислению алюминия. Но когда мы покрыли алюминий ртутью и под ней поцарапали алюминий, то мы содрав пленку позволили ртути создать сплав с алюминием, то есть ртуть тут же внедряется в кристаллическую решетку алюминия. Теперь самое главное. Оксидная пленка препятствует окислению, а вот то место где мы сделали амальгаму, там алюминий довольно активно будет окисляться кислородом воздуха с образованием белого порошка, так будет продолжаться пока весь слиток алюминия не окислиться. Если положить такой слиток в воду, то он будет очень активно окисляться и там, вытесняя из воды водород. реакция в воде протекает настолько бурно, что происходит взрыв.
Чтобы взрыва не было и чтобы можно было контролировать выход количества водорода, можно не класть слиток в воду, а продувать мимо такого слитка водяной пар, который будет окисляться до водорода, то есть алюминий будет отнимать у пара кислород, а водород будет побочным продуктом, который Вы запросто можете использовать в качестве топлива для авто.
Алюминий можно добывать повсюду, на свалках, на помойках, можно даже открыть нелегальный приемный пункт, в любом случае при всех затратах, этот метод окупиться с лихвой, это будет самое дешевое и легко добываемое топливо.
Представьте что у Вас на авто стоит некий герметичный бачок, который Вы можете открыть и бросить туда алюминиевую вилку, ложку или кастрюлю или кучу алюминиевых проводов, естественно вначале следует купить градусник и ртуть из него нанести на алюминий выше упомянутым способом. Для удобства можно плавить алюминиевый хлам и отливать из него компактные заготовки, потом создать на слитке хотя бы маленькую точку амальгамы, а после покрыть это место замазкой или скотчем, или просто положить в целлофановый пакет и плотно завязать его, чтобы не было реакции окисления. Вот такие заготовки потом Вы можете кидать в герметично закрывающийся бачок, потом подавать туда пар и получать на выходе чистый водород, который будет питать Ваше авто. метод взрыво безопасен, так как количество выделенного водорода зависит от количества поданного пара. распологать такой «реактор» можно непосредственно перед камерой куда будет впрыскиваться водород, чтобы выделяющийся водород, сразу же использовался не образуя больших взрывоопасных скоплений.
Этот метод вполне реален.
Кто не верит, читайте школьный учебник химии.
Изготовлен генератор, представляющий собой герметичную емкость с внутренним объемом 220 мл и отделяемой крышкой, в которой находятся герметичные, изолированные токоподводы-крепления для алюминия и газоотводная трубка для отвода водорода. В генератор заливают 200 г раствора поваренной соли концентрацией 17 Закрепляют к токоподводам-креплениям алюминиевые пластины площадью 13 см 2 каждая. Закрывают генератор крышкой, убедясь в герметичности. После чего подают напряжение на токоподводы. Для более быстрого удаления оксидной пленки с поверхности алюминия в начале подается напряжение до 1,5 В. После деструкции оксидной пленки понижают напряжение до рабочей величины. Для работы генератора выбран диапазон напряжений 0,3-1,5 В, так как при этих значениях напряжения характеристика G/W), выше, чем при больших или меньших значениях напряжения, что позволяет более рационально использовать электроэнергию, но генератор водорода может работать и в более широком диапазоне напряжений.
Предлагаемый способ можно реализовать более эффективно
Для увеличения выхода водорода при тех же значениях мощности можно применить многоэлектродную систему в одной ячейке три электрода между отрицательным и положительным электродами располагается пассивный электрод, и так две ячейки, получен более высокий результат. Также в качестве восстановителя можно использовать дисперсный алюминий, что позволяет повысить выход водорода.
В результате испытания генератора по методике примера 1 заливают в генератор с двумя алюминиевыми электродами 200 г морской воды. Полная площадь каждого электрода 13 см 2. В результате получены следующие результаты: выход водорода при 1,5 В 0,5 л/ч, выход относительно энергии при 1,5 В 0,52 Вт/ч.
При увеличении общей концентрации солей упариванием увеличивается выход водорода во времени и относительно затраченная энергия достигает максимума 16-23 солей морской воды. Данный способ позволяет обеспечить равномерное получение водорода и позволяет регулировать его выход с требуемым потребителю расходом.
Формула изобретения
Способ получения водорода, включающий взаимодействие алюминия с водным раствором галогенида щелочного или щелочноземельного металла, отличающийся тем, что, с целью обеспечения возможности регулирования выхода водорода, взаимодействие осуществляют при одновременном пропускании электрического тока через реакционную смесь сначала при напряжении 1,5 В, а после удаления оксидной пленки напряжение снижают до 0,3 В.
Получение водорода в домашних условиях
 Способ 1.
Насыпаем в колбу небольшое количество едкого кали либо натра и заливаем 50 -100 мл воды, перемешиваем раствор до полного растворения кристаллов. Далее добавляем несколько кусочков алюминия. Сразу же начнется реакция с выделением водорода и тепла, сначала слабая, но постоянно усиливающаяся.
Способ 1.
Насыпаем в колбу небольшое количество едкого кали либо натра и заливаем 50 -100 мл воды, перемешиваем раствор до полного растворения кристаллов. Далее добавляем несколько кусочков алюминия. Сразу же начнется реакция с выделением водорода и тепла, сначала слабая, но постоянно усиливающаяся.
Дождавшись пока реакция будет происходить более активно, аккуратно добавим еще 10г. щелочи и несколько кусочком алюминия. Так мы значительно усилим процесс. Закупориваем колбу, пробиркой с трубкой ведущей сосуд для сбора газа. Ждем примерно 3 -5 мин. пока водород вытеснит воздух из сосуда.
Как образуется водород? Оксидная пленка, которая покрывающая поверхность алюминия, при контакте с щелочью разрушается. Так как алюминий является активным металлом, то он начинает реагировать с водой, растворяясь в ней, при этом выделяется водород.
2Al + 2NaOH + 6h3O → 2Na + 3h3
Способ 2. Водород из алюминия, сульфата меди и пищевой соли.
В колбу насыпаем немного сульфата меди, и соли. Добавляем воду и перемешиваем до полного растворения. Раствор должен, окрасится в зеленый цвет, если этого не произошло, добавьте еще небольшое количество соли. Колбу необходимо поставить в чашку наполненной холодной водой, т.к. при реакции, будет выделятся большое количество тепла. Добавляем в раствор несколько кусочков алюминия. Начнется реакция.
Как происходит выделение водорода? В процессе образуется хлорид меди, смывающий оксидную пленку с метала. Одновременно с восстановлением меди происходит образование газа.
Способ 3. Водород из цинка и соляной кислоты.
Помещаем в пробирку кусочки цинка и заливаем их соляной кислотой. Являясь активным металлом цинк, взаимодействуя с кислотой, вытесняет из нее водород.
Zn + 2HCl → ZnCl2 + h3
Способ 4. Производство водорода электролизом.
Пропускаем через раствор воды и проваренной соли электрический ток. При реакции, будет выделятся водород и кислород.
Водород уже достаточно давно рассматривается и кое-где используется в качестве экологически чистого вида топлива. Но более широкому использованию водородного топлива мешает целый ряд неразрешенных на сегодняшний день проблем, главными из которых являются хранение и транспортировка. Однако, группа исследователей из американской Армейской научно-исследовательской лаборатории, проводя эксперименты на Абердинском испытательном полигоне близ Мериленда, сделала случайное открытие. Пролив воду на брусок особого алюминиевого сплава, состав которого держится пока в секрете, исследователи заметили мгновенно начавшийся процесс бурного выделения водорода.
Из школьного курса химии, если кто его еще помнит, водород является побочным продуктом реакции между водой и алюминием. Однако, данная реакция обычно протекает лишь при достаточно высокой температуре или в присутствии специальных катализаторов. Да и тогда она идет достаточно "неторопливо", на заполнение бака водородного автомобиля потребуется около 50 часов, а энергетическая эффективность такого метода получения водорода не превышает 50 процентов.
Все вышесказанное не имеет отношения к реакции, в которой принимает участие новый сплав алюминия. "Эффективность этой реакции вплотную приближается к 100 процентам, а сама реакция "разгоняется" до максимальной производительности менее, чем за три минуты" - рассказывает Скотт Грендаль, руководитель научной группы.
Использование системы, вырабатывающей водород по мере необходимости, решает массу имеющихся проблем. Воду и алюминиевый сплав легко транспортировать из одного места в другое, оба этих вещества сами по себе инертны и стабильны. Во-вторых, для начала реакции не требуется никакого катализатора, ни первоначального толчка, реакция начинает идти сразу же, как вода входит в контакт со сплавом.
Все вышесказанное еще не означает, что исследователи обнаружили панацею в области водородного топлива. В этом деле существует еще целый ряд вопросов, подлежащих выяснению или уточнению. Первым вопросом является то, будет ли работать такая схема получения водорода вне лаборатории, ведь существует множество примеров, когда экспериментальные технологии отлично работают в лабораторных условиях, но терпят полную неудачу при полевых испытаниях. Вторым вопросом является вопрос сложности и стоимости производства алюминиевого сплава, стоимость утилизации продуктов реакции, которые станут факторами, определяющим экономическую целесообразность нового способа получения водорода.
И в заключение следует отметить, что на выяснение упомянутых выше вопросов, скорее всего, уйдет не так уж и много времени. И только после этого можно будет сделать выводы о дальнейшей жизнеспособности нового метода получения водородного топлива.
Источники: www.ntpo.com, all-he.ru, h3-o.sosbb.net, 505sovetov.ru, dailytechinfo.org, joyreactor.cc
Кракен – гигантский осьминог
Гигантские крысы
Загадочные вирусы
Видение Джуд-Хаэля. Девушка с небес
Где предпочтительно остановиться в Москве

Москва - огромный мегаполис, ежедневно встречающий многочисленных приезжих. Кто-то отправляется сюда с экскурсионным визитом, у кого-то цель – деловая поездка. Удобство...
Китайская культура - древняя цивилизация

Согласно утверждению китайского ученого Лян Цичао, Китай вместе с Вавилоном, Индией и Египтом является одной из четырех древних цивилизаций. Эта большая...
Философия Древнего Востока

Особенности направлений древнеиндийской философии: брахманизм; философия эпического периода; неортодоксальные и ортодоксальные школы. Школы и направления древнекитайской философии: конфуцианство; даосизм; моизм; легизм; ...
Водород - широко распространенный элемент. Благодаря своей уникальности он может выступать в качестве окислителя и в качестве восстановителя. Существует несколько методов получения водорода .
Промышленный метод получения водорода.
1. Электролиз водных растворов солей (поваренная соль NaCl ).
2. Пропускание паров поды над раскаленным коксом (Т = 1000 °С):
H 2 O + C = H 2 + CO ,
Реакция обратима!
Смесь (Н 2 , СО и Н 2 О ) называется водяным газом.
А на 2-ой стадии водяной газ пропускают над оксидом железа (III) при температуре около 450°С:
СО + Н 2 О = СО 2 + Н 2 ,
Часто эту реакцию называют реакцией сдвига.
3. Получение из природного газа. Основа - конверсия метана (основной компонент природного газа, СН 4 ) с водяным паром. В итоге получается обратимая смесь, которая называется синтез-газом. Условия протекания процесса: никелевый катализатор и 1000°С:
СН 4 + Н 2 О = СО 2 + 3Н 2 ,
Эту реакцию часто используют для получения водорода для реакции Габера (синтез аммиака).
4. Крекинг нефтяных продуктов.
Лабораторный метод получения водорода.
1. Под воздействием разбавленных кислот на металлы, которые стоят в ряду напряжения левее водорода.
Zn + HCl = ZnCl 2 + H 2 ,
2. Электролиз растворов кислот, щелочей на катоде выделяется водород.
3. Действие щелочей на цинк или алюминий:
2Al + 2NaOH + 6H 2 O = 2Na + 3H 2
4. Гидролиз гидридов:
NaH + H 2 O = NaOH + H 2 ,
5. Реакция кальция с водой:
Ca + 2H 2 O = Ca(ОН) 2 + H 2 .
Водород уже достаточно давно рассматривается и кое-где используется в качестве экологически чистого вида топлива . Но более широкому использованию водородного топлива мешает целый ряд неразрешенных на сегодняшний день проблем, главными из которых являются хранение и транспортировка. Однако, группа исследователей из американской Армейской научно-исследовательской лаборатории, проводя эксперименты на Абердинском испытательном полигоне близ Мериленда, сделала случайное открытие. Пролив воду на брусок особого алюминиевого сплава, состав которого держится пока в секрете, исследователи заметили мгновенно начавшийся процесс бурного выделения водорода.
Из школьного курса химии, если кто его еще помнит, водород является побочным продуктом реакции между водой и алюминием. Однако, данная реакция обычно протекает лишь при достаточно высокой температуре или в присутствии специальных катализаторов. Да и тогда она идет достаточно "неторопливо", на заполнение бака водородного автомобиля потребуется около 50 часов, а энергетическая эффективность такого метода получения водорода не превышает 50 процентов.
Все вышесказанное не имеет отношения к реакции, в которой принимает участие новый сплав алюминия. "Эффективность этой реакции вплотную приближается к 100 процентам, а сама реакция "разгоняется" до максимальной производительности менее, чем за три минуты" - рассказывает Скотт Грендаль (Scott Grendahl), руководитель научной группы.
Использование системы, вырабатывающей водород по мере необходимости, решает массу имеющихся проблем. Воду и алюминиевый сплав легко транспортировать из одного места в другое, оба этих вещества сами по себе инертны и стабильны. Во-вторых, для начала реакции не требуется никакого катализатора, ни первоначального толчка, реакция начинает идти сразу же, как вода входит в контакт со сплавом.
Все вышесказанное еще не означает, что исследователи обнаружили панацею в области водородного топлива. В этом деле существует еще целый ряд вопросов, подлежащих выяснению или уточнению. Первым вопросом является то, будет ли работать такая схема получения водорода вне лаборатории, ведь существует множество примеров, когда экспериментальные технологии отлично работают в лабораторных условиях, но терпят полную неудачу при полевых испытаниях. Вторым вопросом является вопрос сложности и стоимости производства алюминиевого сплава, стоимость утилизации продуктов реакции, которые станут факторами, определяющим экономическую целесообразность нового способа получения водорода.
И в заключение следует отметить, что на выяснение упомянутых выше вопросов, скорее всего, уйдет не так уж и много времени. И только после этого можно будет сделать выводы о дальнейшей жизнеспособности нового метода получения водородного топлива.
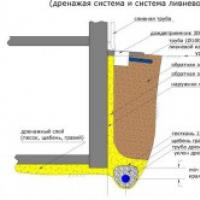 Пристенный дренаж фундамента цена Материалы и инструменты
Пристенный дренаж фундамента цена Материалы и инструменты Расстояние между колодцем и выгребной ямой: нормы СанПиН и СНиП Выгребная яма в многоквартирном доме
Расстояние между колодцем и выгребной ямой: нормы СанПиН и СНиП Выгребная яма в многоквартирном доме Установка стиральной машины и подключение к водопроводу
Установка стиральной машины и подключение к водопроводу Регулировка терморегулятора холодильника своими руками Самодельный термостат для холодильника на дискретных элементах
Регулировка терморегулятора холодильника своими руками Самодельный термостат для холодильника на дискретных элементах Мангал - коптильня из газовых баллонов своими руками Коптильня из пропанового баллона своими руками
Мангал - коптильня из газовых баллонов своими руками Коптильня из пропанового баллона своими руками Детский веломобиль своими руками - подробное описание и схема
Детский веломобиль своими руками - подробное описание и схема Способы сварки медных проводов Точечная сварка медных проводов
Способы сварки медных проводов Точечная сварка медных проводов